近日,我校理學院季一兵、李瑞軍團隊在共識期刊理學學科頂尖期刊Chemical Engineering Journal上連續發表了題為“Laccase-mimicking active inorganic organic hybrid covalent organic framework filtration membrane for rapid removal of drug pollutants”和“Exploring of laccase-like nanozyme and membrane filters for efficient removal of tetracycline hydrochloride”的最新研究成果。
由于藥物的持續使用,包括廢水和水生生態系統在內的各種水環境中檢測到數種類藥物。去除它們的傳統方法(如物理吸附、電化學過程和離子交換)通常需要大量的能源消耗并產生有毒副產物。相比之下,各種生物材料具有更高的去除效率并具有避免產生劇毒副產物的優點。漆酶是該領域的“明星產品”,但其“易碎性”進一步限制了規模化的實際應用。設計出具有漆酶模擬活性的材料是克服惡劣操作條件和擴大應用模式的主要策略之一。
為解決上述問題,研究團隊基于“原位”和“受限配位”的概念設計了一種具有顯著漆酶模擬活性的無機–有機雜化共價有機框架(Cu-BSA@COF)。牛血清白蛋白(BSA)與銅(Cu)的配位結合促進了多銅活性中心的形成(圖1)。COF的骨架和孔隙結構保護活性位點并增強底物吸附。它們之間的協同作用確保材料在各種惡劣操作條件下保持催化活性。研究表明Cu-BSA@COF具有和天然漆酶相接近的底物親和力(Km)和生物催化效率(Kcat/Km)。與天然漆酶和Cu-BSA相比,其生物催化效率分別增加了18.56%和168.57%,結果表明Cu-BSA@COF是天然漆酶的理想替代品。基于上述優勢,研究團隊成功將其與膜技術結合,在最佳工藝和應用條件下,該膜一次過濾可去除90%以上的鹽酸四環素(TC)、對乙酰氨基酚(APAP)、卡馬西平(CBZ)和磺胺甲惡唑(SMZ)(環境中藥物污染物的主要成分)(圖2)。廣泛的適用性和有效規避對環境的次生污染風險為藥物污染物的去除提供了研究新范式。
本研究得到了江蘇省研究生科研與實踐創新計劃項目(KYCX25_1072)和江蘇省重點研發計劃(社會發展)項目(BE2019717)的資助。理學院2022級博士生穆琦瑄和2022級碩士生李心悅為本文共同第一作者,理學院季一兵教授、李瑞軍副教授為本文的共同通訊作者。

圖1:Cu-BSA@COF的合成及部分表征
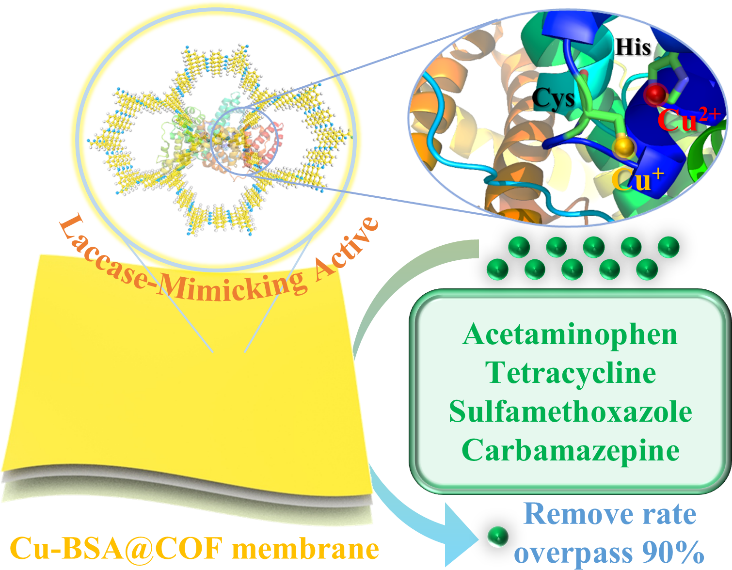
圖2:Cu-BSA@COF膜去除藥物污染物示意圖
論文鏈接:
https://doi.org/10.1016/j.cej.2025.166344
另外,受天然漆酶活性中心的啟發,以Cu2+為活性中心,2-氨基咪唑及谷胱甘肽(GSH)為配體,設計了一種具有高活性、高穩定性的類漆酶活性納米酶(GA-Cu納米酶)。金屬納米酶在使用過程中存在回收困難、易造成二次污染等問題。為了克服此問題,團隊提出通過真空輔助抽濾的方式將GA-Cu納米酶負載到尼龍膜上,使用殼聚糖作為粘合劑,形成致密穩定的復合膜(GA-Cu@CS/GA-Cu/nylon膜)(圖3)。使用復合膜對鹽酸四環素(TC)進行降解研究。結果顯示,一次過濾可降解約80%TC。用LC-MS對主要轉化產物進行鑒定,提出三種TC可能的生物轉化途徑(圖4)。與現有的污染物處理方法相比,GA-Cu@CS/GA-Cu/nylon膜有望在工業上實現大規模、低污染、低能耗和污染物的連續處理。中國藥科大學理學院碩士研究生王云為本文第一作者,理學院李瑞軍副教授和季一兵教授、中科院蘭州化學所海軍研究員為共同通訊作者,中國藥科大學為第一通訊單位。
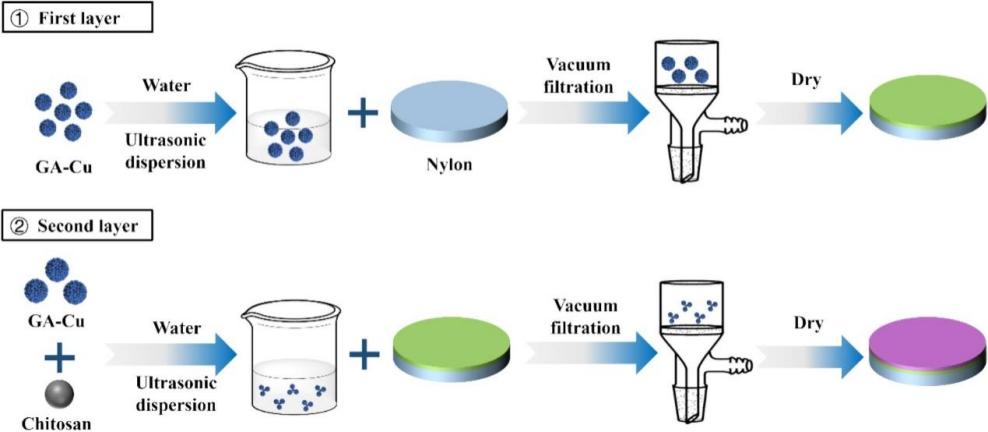
圖3.GA-Cu@CS/GA-Cu/nylon膜的制備示意圖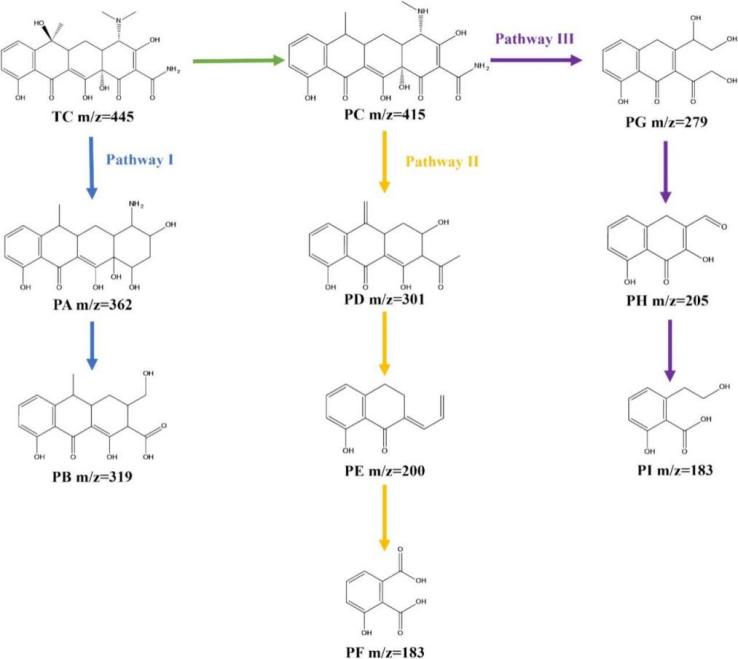
圖4. GA-Cu 納米酶對TC的可能降解途徑
論文鏈接:
https://doi.org/10.1016/j.cej.2024.158021
(供稿單位:理學院,撰寫人:韓佳奇,審稿人:劉帆)





