近日,材料學領(lǐng)域權(quán)威期刊Nano Letters(IF:12.279)在線發(fā)表了中國藥科大學藥學院姚靜教授團隊的最新研究成果——Transforming Complexity to Simplicity: Protein-Like Nanotransformer for Improving Tumor Drug Delivery Programmatically(https://dx.doi.org/10.1021/acs.nanolett.9b05008)。師資博士后熊慧為本文的第一作者,姚靜教授為本文的通訊作者。
納米藥物遞送系統(tǒng)通過提高藥物遞送效率可以改善腫瘤藥物的治療效率。然而,網(wǎng)狀內(nèi)皮系統(tǒng)的清除、腫瘤組織深層滲透困難、腫瘤細胞攝取效率較低、溶酶體中的藥物失活以及釋藥遲滯等體內(nèi)遞藥屏障或技術(shù)壁壘仍然制約著納米藥物的發(fā)展。根據(jù)木桶定律,納米藥物在穿越上述屏障的任一環(huán)節(jié)受阻均會降低藥物的總體遞送效率,從而削弱藥物的最終治療效果。盡管腫瘤微環(huán)境響應(yīng)型的納米藥物遞送系統(tǒng),可以通過多次轉(zhuǎn)換其親疏水性或者尺寸大小以逐層貫穿這些遞藥屏障,然而以往藥物遞送系統(tǒng)的構(gòu)建往往需要依賴于結(jié)構(gòu)復雜且未經(jīng)FDA批準的新型合成生物材料。此外,其所含敏感鍵多依賴于化學或者生物反應(yīng)的完全發(fā)生。因此,這些遞藥系統(tǒng)產(chǎn)業(yè)轉(zhuǎn)化技術(shù)壁壘大且敏感型轉(zhuǎn)換效率仍然受限。為解決上述問題,姚靜教授團隊受蛋白質(zhì)變性和復性的啟發(fā),開發(fā)了一種具有質(zhì)子觸發(fā)的親疏水-尺寸轉(zhuǎn)換特性及光熱療法(PT)介導的腫瘤深部遞送效應(yīng)的瞬時轉(zhuǎn)換納米組裝體。該瞬時轉(zhuǎn)換納米組裝體的構(gòu)建,僅需以FDA批準的藥物阿霉素,單寧酸和吲哚菁綠為構(gòu)建單元,經(jīng)π-π相互作用及靜電作用組裝為DTIG納米轉(zhuǎn)換體。研究表明,DTIG納米轉(zhuǎn)換體在血液循環(huán)的中性環(huán)境下為親水性且具有良好的穩(wěn)定性,而在腫瘤微環(huán)境(pH6.5)及酸性溶酶體內(nèi)(pH4.5)由于質(zhì)子的觸發(fā)可瞬時轉(zhuǎn)換為疏水性大尺寸納米顆粒,在DTIG納米轉(zhuǎn)換體撕裂溶酶體膜發(fā)生逃逸后進入細胞質(zhì)環(huán)境時可再次快速恢復親水性小尺寸特性,從而達到連續(xù)貫穿遞藥生物屏障的效果。該DTIG納米組裝體結(jié)合激光治療具有良好的化療與PT聯(lián)合治療效果以及腫瘤深層藥物滲透效應(yīng),且可以有效改善預后。本研究為開發(fā)納米藥物提供了一種程序化地突破不同的腫瘤靶向藥物遞送屏障的新策略。
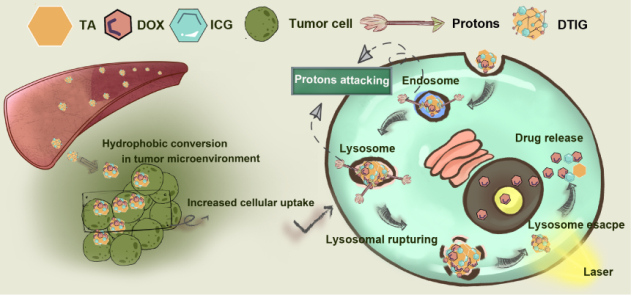
納米藥物DTIG的遞藥作用機制
(供稿單位:藥學院,撰寫人:熊慧、王子函,審核人:吳旻玥)





