近日,我校生命科學(xué)與技術(shù)學(xué)院高向東、尹駿團(tuán)隊(duì)在國(guó)際著名期刊Advanced Functional Materials(IF=19.924)、Journal of Controlled Release(IF=11.467)和Acta Biomaterialia(IF=10.633)發(fā)表系列文章報(bào)道了課題組自主開發(fā)的聚多肽的最新研究成果。
Advanced Functional Materials:
當(dāng)前針對(duì)生物大分子的研究絕大多數(shù)集中在細(xì)胞外靶點(diǎn),而位于細(xì)胞內(nèi)的蛋白質(zhì)和基因靶點(diǎn)卻很少被開發(fā)。本團(tuán)隊(duì)設(shè)計(jì)了一種由pH敏感型電荷屏蔽序列、蛋白酶裂解位點(diǎn)以及超電荷聚多肽三部分組成的腫瘤靶向細(xì)胞內(nèi)遞送系統(tǒng)(activatable supercharged polypeptide, ASCP),實(shí)現(xiàn)在體內(nèi)外將各種生物活性物質(zhì)(包括多肽、蛋白、小分子化合物、siRNA)遞送進(jìn)入細(xì)胞質(zhì)內(nèi),并發(fā)揮其生物功能。相關(guān)內(nèi)容以“A Versatile Platform for the Tumor-Targeted Intracellular Delivery of Peptides, Proteins, and siRNA”為題,長(zhǎng)文形式發(fā)表在Advanced Functional Materials。我校博士研究生楊逸凡、碩士研究生朱海朝為本文共同第一作者,高向東教授、尹駿副研究員和姚文兵教授為本文共同通訊作者。中國(guó)藥科大學(xué)為本文唯一通訊單位。
(全文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202301011)
Journal of Controlled Release:
雙特異性T細(xì)胞激活劑(BiTE)抗體可以重定向T細(xì)胞到腫瘤細(xì)胞,并啟動(dòng)靶向溶解腫瘤細(xì)胞。然而,由于血漿半衰期短、“非靶向”效應(yīng)和PD-1/PD-L1軸免疫抑制等問題,在實(shí)體腫瘤中使用BiTE一直具有挑戰(zhàn)性。本團(tuán)隊(duì)設(shè)計(jì)了一種腫瘤微環(huán)境特異性激活的雙特異抗體平臺(tái)PAPB:Protease-Activated PSTAGylated BiTE,其中包括聚多肽(PSTAG)、蛋白酶激活連接器和BiTE核心。BiTE核心由兩個(gè)針對(duì)PD-L1和CD3的scFv組成。相關(guān)內(nèi)容以“Microenvironment-responsive anti-PD-L1 × CD3 bispecific T-cell engager for solid tumor immunotherapy” 為題,長(zhǎng)文形式發(fā)表在Journal of Controlled Release。我校博士后劉定康為本文第一作者,尹駿副研究員和高向東教授為本文共同通訊作者。中國(guó)藥科大學(xué)為本文唯一通訊單位。
(全文鏈接:https://www.sciencedirect.com/science/article/abs/pii/S0168365923000500?via%3Dihub)
Acta Biomaterialia:
雖然聚乙二醇化(PEGylation)已被廣泛應(yīng)用,但PEG仍具有免疫原性和不可生物降解的問題。為了克服這些問題開發(fā)出多種模擬PEG的聚多肽,其本質(zhì)為蛋白質(zhì),具有長(zhǎng)度可調(diào)節(jié)、生物可降解、免疫原性低、易于生產(chǎn)等特性,是提高生物大分子成藥性的研究熱點(diǎn)之一。本團(tuán)隊(duì)在自主開發(fā)的聚多肽的基礎(chǔ)上系統(tǒng)總結(jié)了聚多肽的發(fā)展、設(shè)計(jì)和生物化學(xué)特性,介紹了其在延長(zhǎng)多肽、蛋白質(zhì)、抗體片段和納米載體半衰期中的應(yīng)用,討論了其作為“隱身”生物聚合物、多分子銜接器和細(xì)胞內(nèi)遞送載體等最新研究成果。相關(guān)內(nèi)容以“Unstructured Polypeptides as a Versatile Drug Delivery Technology”為題,綜述形式發(fā)表在Acta Biomaterialia。我校博士研究生嵇悅、博士后劉定康為本文共同第一作者,尹駿副研究員和高向東教授為本文共同通訊作者。中國(guó)藥科大學(xué)為本文唯一通訊單位。
(全文鏈接:https://www.sciencedirect.com/science/article/abs/pii/S1742706123002106)
以上工作得到了國(guó)家自然科學(xué)基金項(xiàng)目、江蘇省自然科學(xué)基金項(xiàng)目、新疆維吾爾自治區(qū)重點(diǎn)研發(fā)計(jì)劃項(xiàng)目、“雙一流”學(xué)科創(chuàng)新團(tuán)隊(duì)的資助。
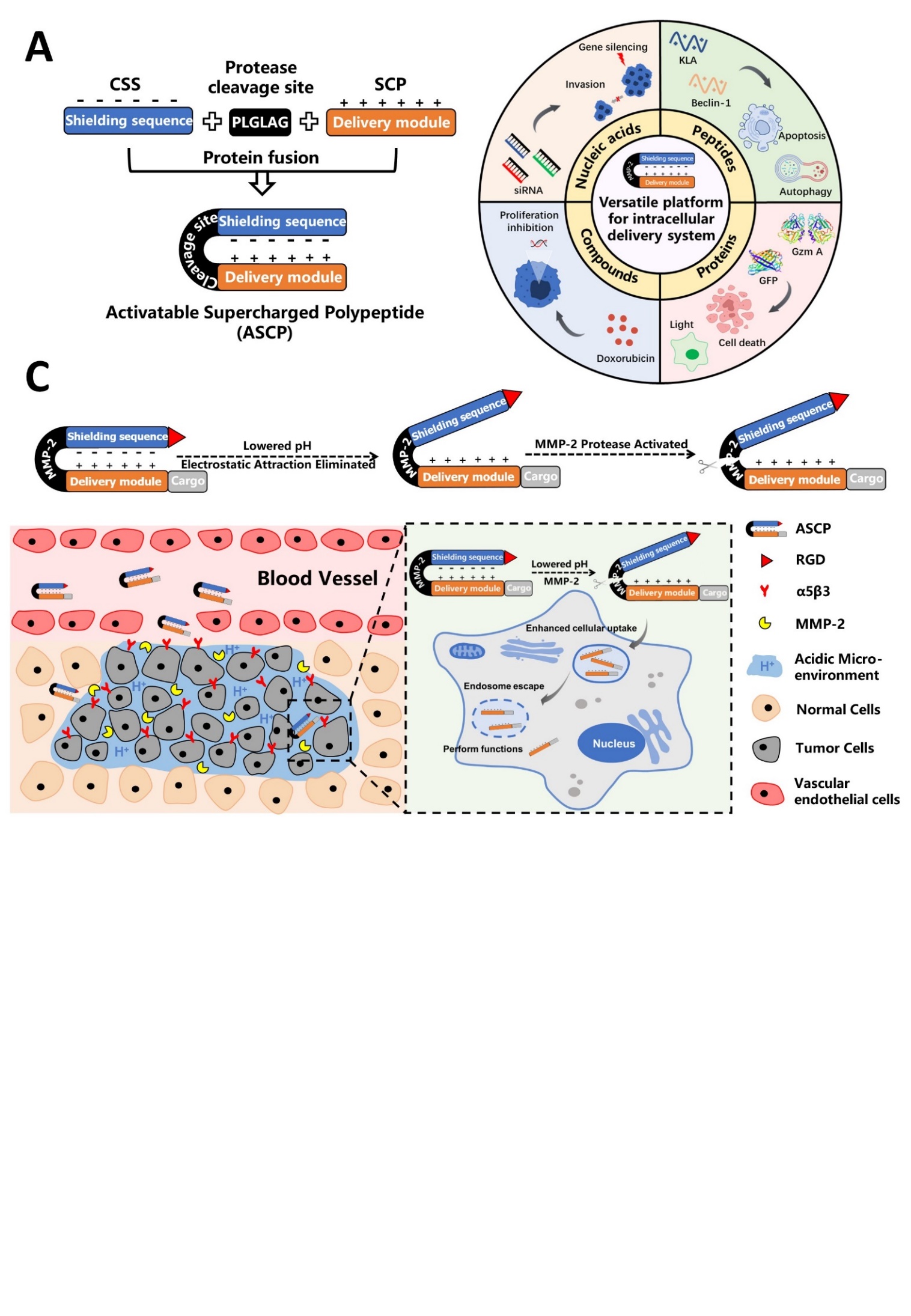
圖1
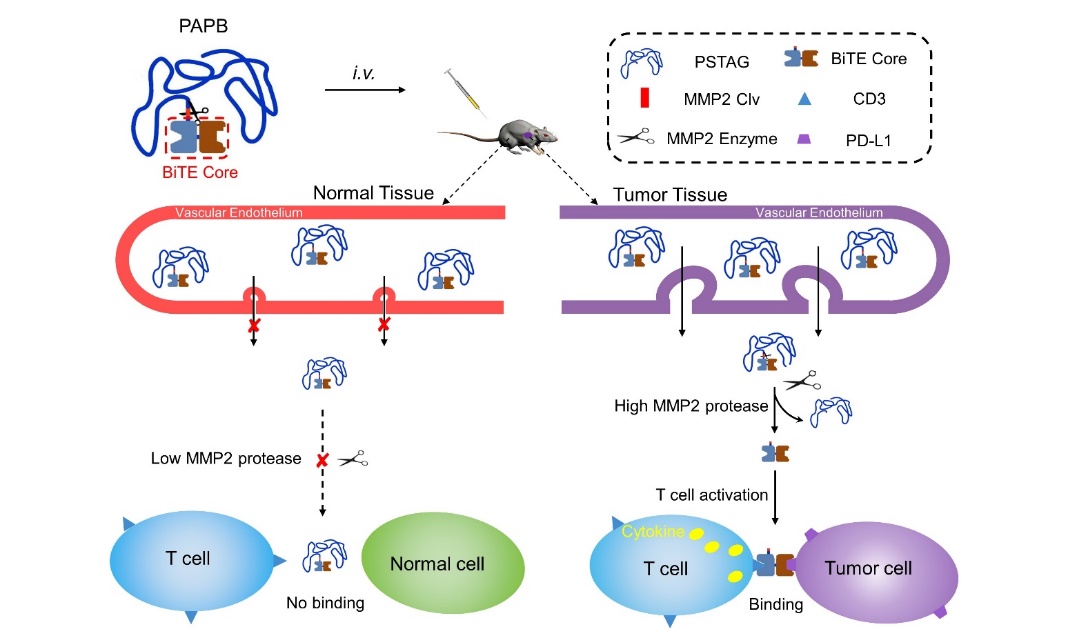
圖2
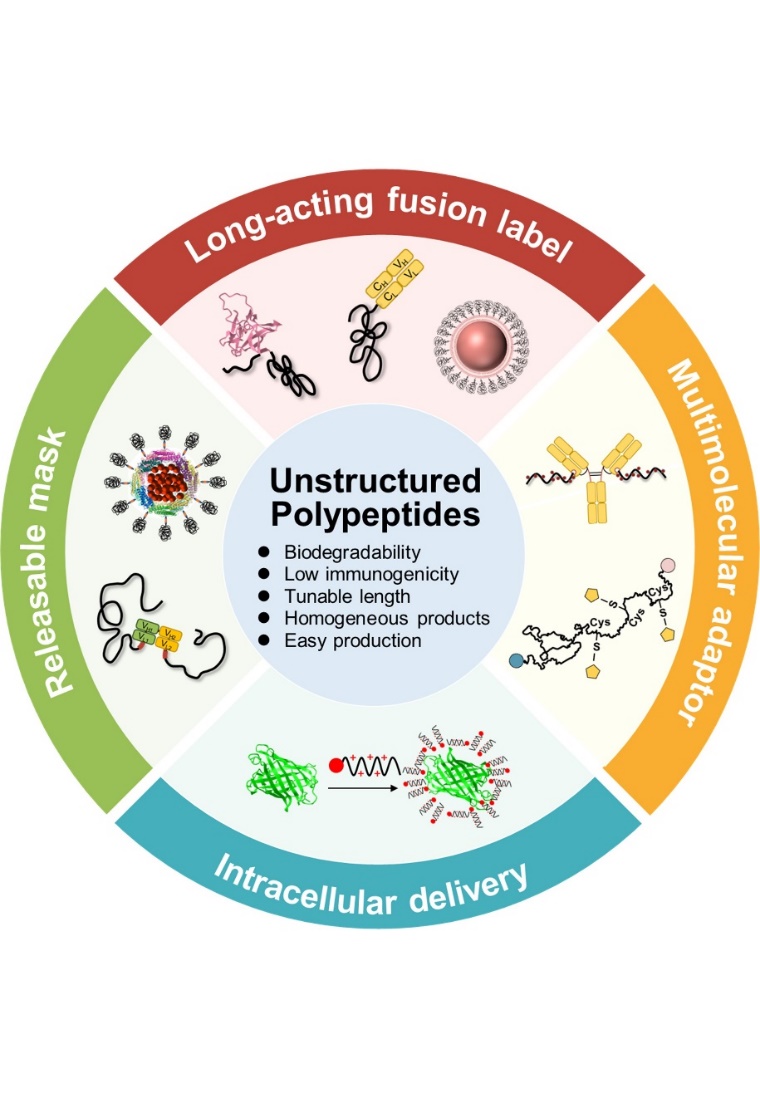
圖3
(供稿單位:生命科學(xué)與技術(shù)學(xué)院,撰寫人:羅鴻,審稿人:黃欣、周天健)





