近日,權(quán)威期刊Advanced Materials(IF:32.086)在線發(fā)表藥學(xué)院劉東飛教授團(tuán)隊(duì)的最新研究論文:Controlled Interfacial Polymer Self-assembly Coordinates Ultrahigh Drug Loading and Zero-Order Release in Particles Prepared under Continuous Flow。我校與芬蘭赫爾辛基大學(xué)聯(lián)合培養(yǎng)的張佩博士、藥學(xué)院碩士研究生劉穎欣和博士研究生馮國(guó)兵為本文共同第一作者。我校藥學(xué)院劉東飛教授和荷蘭格羅寧根大學(xué)Helder A. Santos教授為本文共同通訊作者,主要合作者還包括南京醫(yī)科大學(xué)附屬第一醫(yī)院凡進(jìn)教授、沈陽(yáng)藥科大學(xué)權(quán)鵬教授、芬蘭赫爾辛基大學(xué)副校長(zhǎng)Jouni Hirvonen。中國(guó)藥科大學(xué)為本文第一通訊單位。
藥物與輔料經(jīng)過(guò)特定包載工藝制成微球、納米粒、脂質(zhì)體、膠束等微粒后,可有效調(diào)控藥物體內(nèi)吸收和分布,針對(duì)性的改善藥物體內(nèi)動(dòng)力學(xué)特征,提高藥物療效并降低其副作用。高效包載和控釋是微粒制劑實(shí)現(xiàn)藥物體內(nèi)動(dòng)力學(xué)高效調(diào)控的先決條件,但該類(lèi)制劑一直飽受包載藥物種類(lèi)局限、載藥量低、釋放控制精準(zhǔn)度差等共性問(wèn)題的困擾,致使其臨床價(jià)值未能得到充分挖掘和彰顯。基礎(chǔ)研究是解決微粒制劑工程難題的總開(kāi)關(guān),微粒制劑藥物包載及控釋瓶頸的突破,亟需系統(tǒng)闡明藥物與載體材料的跨尺度作用規(guī)律及機(jī)制,構(gòu)建調(diào)控藥物及載體材料空間分布的核心技術(shù)體系,從而形成微粒制備基礎(chǔ)理論框架。
劉東飛教授團(tuán)隊(duì)將結(jié)構(gòu)及性質(zhì)多樣的藥物分子轉(zhuǎn)換為膠體顆粒作為包載的基本單元,通過(guò)提高聚合物載體材料在藥物膠體顆粒表面和油水界面的分布,制備具有功能基元序構(gòu)特點(diǎn)的微球,實(shí)現(xiàn)多肽蛋白類(lèi)藥物的高效包載和可控釋放。聚合物載體材料在藥物膠體顆粒表面的吸附,有效突破兩者相容性瓶頸,阻斷藥物從油相到水相的轉(zhuǎn)移,實(shí)現(xiàn)高達(dá)99.9%的超高包封效率。通過(guò)水相中鹽的引入,增強(qiáng)聚合物載體材料在油水界面的分布,在微球表面形成致密聚合物層,實(shí)現(xiàn)藥物接近零級(jí)的釋放動(dòng)力學(xué)。結(jié)合分子動(dòng)力學(xué)模擬等手段,本研究初步探究了聚合物分子界面分布對(duì)藥物包封、微球結(jié)構(gòu)與尺寸、藥物釋放的調(diào)控機(jī)制。利用自主開(kāi)發(fā)的連續(xù)流裝置(專(zhuān)利號(hào)CN202111465267)實(shí)現(xiàn)對(duì)微球制備過(guò)程的精準(zhǔn)控制,有效降低所制備微球的批次間差異。本研究進(jìn)一步完善了基于連續(xù)流的高性能載藥微球制備平臺(tái)的核心技術(shù)體系。
以上工作得到了國(guó)家自然科學(xué)基金項(xiàng)目(51903251,81973266,81772352和82072437)、芬蘭科學(xué)院研究基金(322093和331151)、江蘇省杰出青年自然科學(xué)基金(BK20190033)、江蘇省基礎(chǔ)研究計(jì)劃自然科學(xué)基金(BK20190554)、天然藥物活性組分與藥效國(guó)家重點(diǎn)實(shí)驗(yàn)室自主研究課題項(xiàng)目(SKLNMZZ202221)、遼寧省教育廳研究基金(2020LJC04)、赫爾辛基大學(xué)研究基金、HiLIFE研究基金、Sigrid Jusélius基金會(huì)和UMCG研究基金等項(xiàng)目的資助。
文章鏈接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202211254
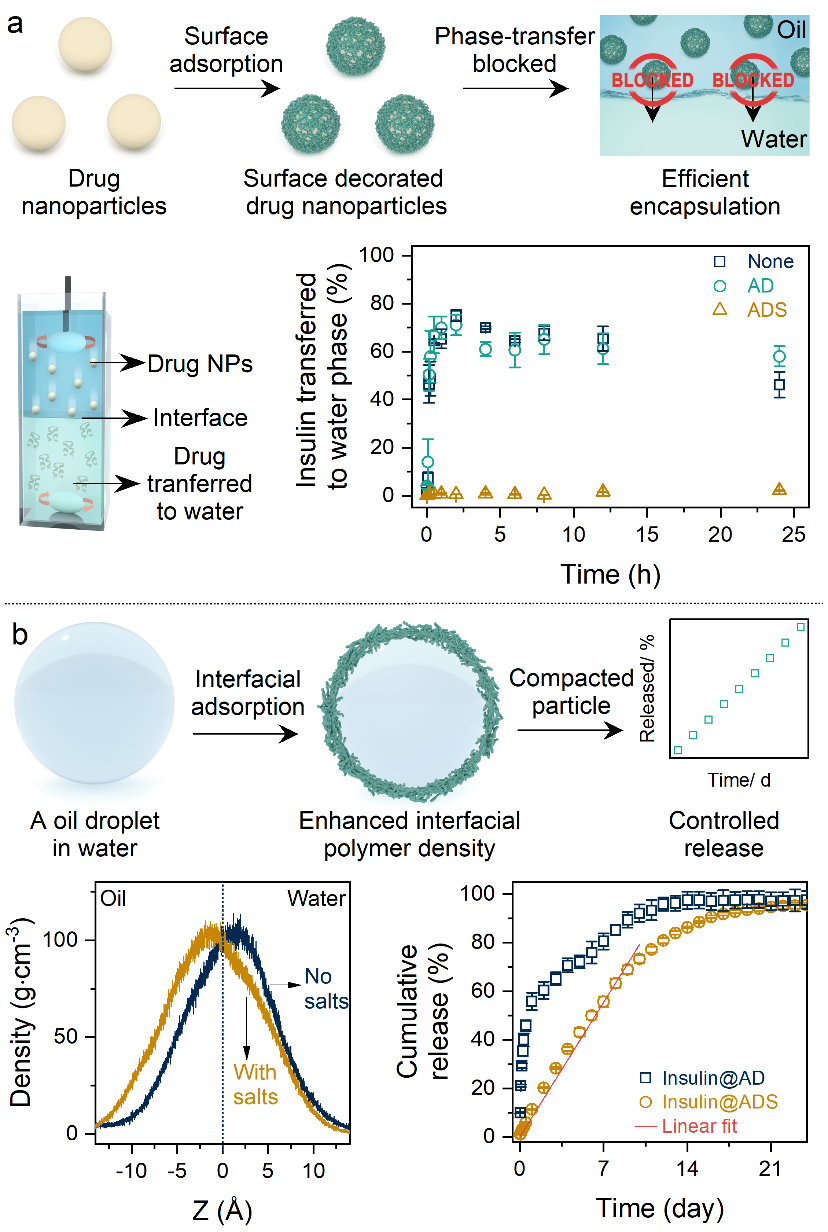
主要結(jié)果匯總示意圖
(供稿單位:藥學(xué)院,撰寫(xiě)人:顧瑜,審稿人:黃欣)





