近日,我校理學院在共識權威期刊Angewandte Chemie International Edition上發表了題為 “Novel Light-Promoted Bioorthogonal Reaction via Molecular Recombination for the Synthesis of Polysubstituted Pyrrole and its Application in Vitro and in Vivo Studies” 的最新研究成果。2023級碩士生倪傲挺、博士生張晨璐和博士后張男俠為本文的共同第一作者,馮捷副教授、陳亞東教授和陸濤教授為本文的共同通訊作者。
生物正交反應因其高度選擇性、安全高效且不干擾生命體系等特點,近年來在有機化學、藥物研發及化學生物學等領域受到廣泛關注,并已成為推動生物標記與精準治療研究的重要工具。盡管已有多種新型的生物正交反應被相繼報道,但當前大多數方法仍主要基于四嗪類底物或不飽和烴類底物,難以兼顧官能團引入的多樣性、水溶性底物的適應性以及反應體系的廣譜性,亟需發展新的反應體系以滿足更復雜的生物環境應用需求。
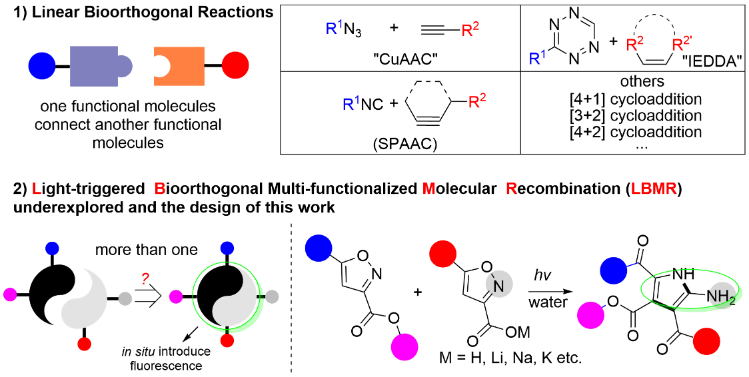
LBMR反應的設計思路和簡介
針對上述挑戰,研究團隊創新性地開發了一種全新的光促進生物正交反應(Light-Promoted Bioorthogonal Reaction via Molecular Recombination, 簡稱 LBMR)。該反應中異噁唑-3-甲酸酯類底物和異噁唑-3-甲酸或其鹽類為底物,在類生物兼容體系中可高效生成多取代吡咯衍生物。該反應過程涉及光誘導的分子重排和重組,具有反應條件溫和、動力學快速、對活性小分子無干擾等優點,展現出良好的底物兼容性與生物體系適應性。
更為重要的是,LBMR反應產物2-氨基吡咯具有天然熒光激發特性,使該反應無需額外引入熒光基團,即可直接用于細胞成像。該方法已成功應用于A549、HUH-7、NUGC3等多種腫瘤細胞的原位熒光標記,為細胞追蹤與生物成像研究提供了簡便高效的新手段。
此外,該反應體系亦在斑馬魚胚胎體內實現了高效的原位熒光標記,進一步驗證了其在體內應用中的潛力,展現出作為化學生物學工具的廣闊前景。
總之,LBMR反應利用光促進的分子重組策略,實現了四取代吡咯類衍生物的快速構建,具備廣泛的底物適應性、良好的生物相容性以及體外和體內成像能力,為現有生物正交化學反應體系提供了有力補充。
該研究工作得到了國家自然科學基金、中國藥科大學“雙一流”建設項目等經費的資助。
(供稿單位:理學院,撰寫人:袁嘉辰,審稿人:劉帆)





